Descubre las 5 partes esenciales del átomo
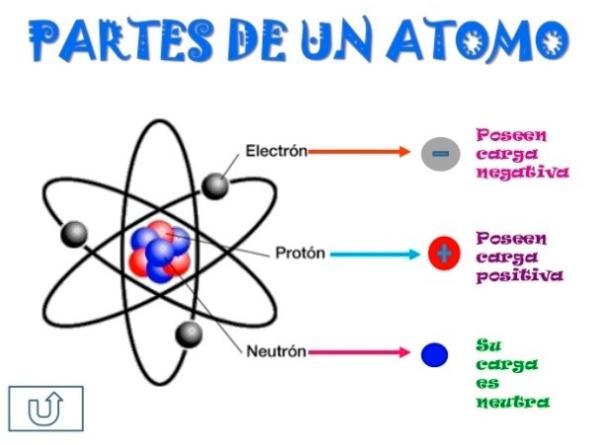
El átomo es la unidad más pequeña de la materia que puede participar en una reacción química y, como tal, es esencial para comprender cómo funciona el mundo que nos rodea. Cada átomo está compuesto por varias partes fundamentales que trabajan en conjunto para darle sus propiedades únicas. En este artículo, exploraremos las cinco partes esenciales del átomo y cómo afectan a su comportamiento.
1. Núcleo
El núcleo es el centro del átomo y está compuesto por protones y neutrones. Los protones tienen carga positiva, mientras que los neutrones no tienen carga. Juntos, los protones y los neutrones forman la mayor parte de la masa del átomo. La cantidad de protones en el núcleo determina el elemento químico al que pertenece el átomo.
2. Electrones
Los electrones son partículas de carga negativa que orbitan alrededor del núcleo en capas llamadas niveles de energía. Los electrones en los niveles de energía más cercanos al núcleo tienen menos energía que los que están más alejados. La cantidad de electrones en las capas exteriores determina cómo el átomo interactúa con otros átomos y cómo se combinan para formar moléculas.
3. Orbitales
Los orbitales son regiones en el espacio alrededor del núcleo donde es más probable que se encuentren los electrones. Cada nivel de energía tiene un número finito de orbitales, y cada orbital puede contener un máximo de dos electrones. La forma del orbital depende del nivel de energía y del tipo de átomo.
4. Carga
La carga del átomo se determina por la cantidad de protones y electrones que tiene. Si el átomo tiene el mismo número de protones y electrones, se dice que es neutro y no tiene carga neta. Si el átomo tiene más protones que electrones, tiene carga positiva y se llama ion positivo. Si tiene más electrones que protones, tiene carga negativa y se llama ion negativo.
5. Isótopos
Los isótopos son átomos del mismo elemento químico que tienen un número diferente de neutrones en el núcleo. Esto significa que tienen la misma cantidad de protones y electrones, pero una masa diferente. Los isótopos pueden ser estables o inestables, y los inestables pueden emitir radiación en forma de partículas o energía.
Conclusión
Comprender las partes esenciales del átomo es crucial para comprender cómo funciona la química y la física. Aunque el átomo es pequeño, está compuesto por partes complejas que interactúan de manera única para darle al átomo sus propiedades únicas. Al estudiar estas partes, podemos aprender cómo los átomos se combinan para formar moléculas y cómo podemos manipularlos para crear nuevos materiales y productos.
Preguntas frecuentes
1. ¿Por qué los electrones no se caen en el núcleo?
Los electrones no se caen en el núcleo debido a la fuerza electromagnética entre ellos y los protones en el núcleo. Esta fuerza mantiene a los electrones en sus órbitas y les impide caer en el núcleo.
2. ¿Por qué los isótopos son importantes?
Los isótopos son importantes porque pueden tener propiedades únicas que los hacen útiles en una variedad de aplicaciones, desde la medicina hasta la energía nuclear. Por ejemplo, algunos isótopos se utilizan en la radioterapia para tratar el cáncer, mientras que otros se utilizan como combustible en reactores nucleares.
3. ¿Cómo se determina el número de electrones en un átomo?
El número de electrones en un átomo se determina por el número de protones en el núcleo. Si el átomo es neutro, tendrá la misma cantidad de protones y electrones. Si el átomo tiene carga positiva, tendrá menos electrones que protones. Si tiene carga negativa, tendrá más electrones que protones.
4. ¿Qué son los iones?
Los iones son átomos que tienen una carga neta diferente de cero debido a una cantidad desigual de protones y electrones. Los iones positivos tienen más protones que electrones, mientras que los iones negativos tienen más electrones que protones.
5. ¿Qué es un orbital?
Un orbital es una región del espacio alrededor del núcleo donde es más probable que se encuentren los electrones. Los orbitales tienen diferentes formas y tamaños y pueden contener un máximo de dos electrones. El número y la disposición de los orbitales dependen del nivel de energía y del tipo de átomo.
Deja una respuesta